Bezahlbarkeit versus Zugang: Wie können wir ein faires System für alle finden?
1. Der Spagat zwischen Regulierung und Zugang
2. Wie hoch ist die Zahlungsbereitschaft für Arzneimittel?
3. Verbessert die EU-Mitgliedschaft den Zugang zu neuen Medikamenten?
1. Wie werden Preise für neue Arzneimittel bestimmt?

Foto: HCHE
ANMOG
Im Jahr 2011 wurde mit dem Arzneimittelmarktneuordnungsgesetz (AMNOG) ein Verfahren zur Preisbestimmung neuer Arzneimittel eingeführt.
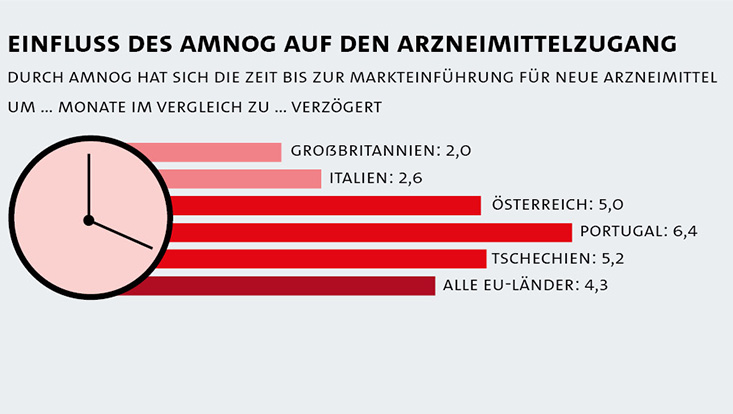
Foto: HCHE
Veränderung der Verfügbarkeit von Arzneimitteln durch AMNOG
Durch die Einführung von ANMOG hat die Zeit bis zur Verfügbarkeit von Arzneimitteln in Deutschland zugenommen.
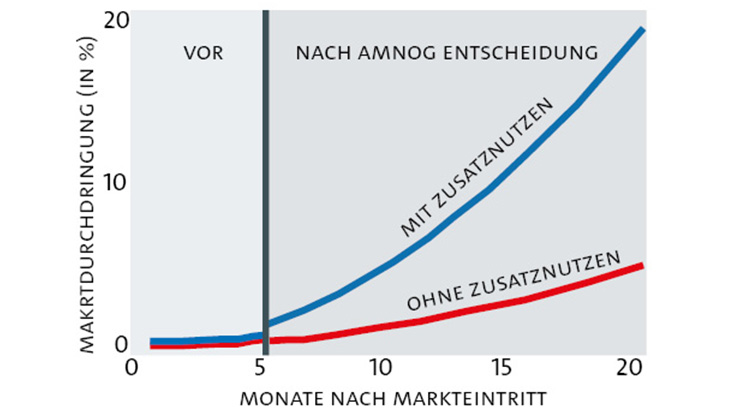
Foto: HCHE
Vorteile trotz verzögertem Markteintritt
„Eine positive Bewertung ist wie eine Qualitätsbewertung. Ärzt:innen verschreiben eher Arzneimittel mit Zusatznutzen als Arzneimittel ohne Zusatznutzen. Dadurch wird die Marktdurchdringung beschleunigt. Dies wirkt der verzögerten Verfügbarkeit entgegen.“
Prof. Dr. Tom Stargardt
2. Wie hoch ist die Zahlungsbereitschaft für Arzneimittel in Deutschland?

Foto: HCHE
Ein genauere Betrachtung ist notwendig
Deutschland verfügt über den größten Arzneimittelmarkt Europas und den drittgrößten Markt weltweit. Wir haben eine hohe Verfügbarkeit von Arzneimitteln und eine schnelle Entscheidung über die Erstattung. Im internationalen Vergleich sind die Ausgaben für Arzneimittel hoch und haben in den letzten Jahren deutlich zugenommen.

Foto: AdobeStock
Zahlungsbereitschaft für ausgewählte Indikationsbereiche
Wir haben die Zahlungsbereitschaft (Willingnes To Pay, kurz "WTP") für neu zugelassene Arzneimittel in drei Indikationsbereichen untersucht: Diabetes, Herz-Kreislauf-Erkrankung und Psoriasis (Schuppenflechte).

Foto: HCHE
Unterschiedliche Bewertungen nach Indikationsgebieten
Der Wert von Behandlungen variiert je nachdem wie Gesundheitsgewinne bei seltenen oder schweren Krankheiten gewichtet werden und wie stark die Zahlungsbereitschaft für Innovationen ist. Zudem können geringe Patientenzahlen oder komplexe Herstellungsverfahren, wie bei Biologika, einen höheren Preis rechtfertigen.
3. Kann die EU-Mitgliedschaft den Zugang zu Arzneimitteln beschleunigen?

Foto: HCHE
Zentralisiertes Zulassungsverfahren
In der EU bietet die Europäische Arzneimittelagentur (EMA, gegründet 1995) ein zentralisiertes Zulassungsverfahren an, um die Qualität, Sicherheit und Wirksamkeit von Arzneimitteln zu gewährleisten. Es ist je nach Indikationsgebiet entweder verpflichtend oder freiwillig. Erfolgreiche Anträge erlauben den Marktzugang zu allen EMA-Ländern.

Foto: HCHE
Auswirkungen der EU-Mitgliedschaft
Wir haben untersucht, ob die EU-Mitgliedschaft Auswirkungen auf den Zugang und die Verfügbarkeit von Arzneimitteln hat. Dies erfolgte auf Basis der EU-Osterweiterung. Grundlage waren die 558 Wirkstoffe, die zwischen 1998 und 2018 in Europa auf den Markt gebracht wurden.

Foto: HCHE
Empfehlungen für eine weitere Beschleunigung des Zugangs
- Ausweitung des verpflichtenden EMA-Anwendungsbereichs auf weitere Wirkstoffe, die derzeit unter den freiwilligen Anwendungsbereich fallen.
- Insbesondere für solche, die finanziell weniger attraktiv sind und von den Herstellern weniger priorisiert werden.
Wo warten Patient:innen in der EU am längsten auf neue Medikamente?
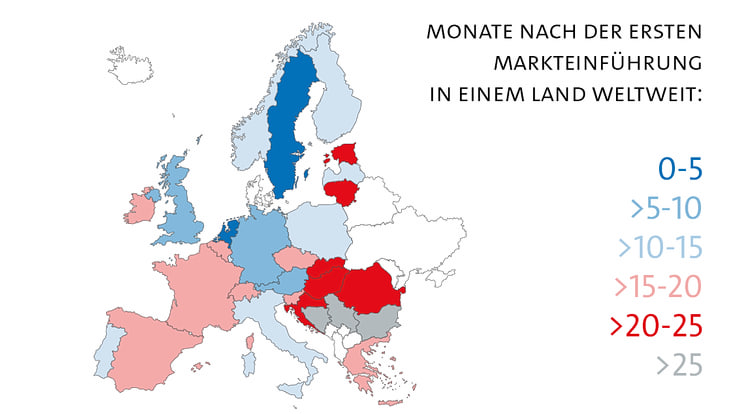
Foto: HCHE
Markteintrittsverzögerung in den EU-Mitgliedstaaten
In der EU bestehen zwischen 0 und 25 Monate Verzögerung bei der Markteinführung neuer Arzneimittel.


